|
��ʡ����������ֱϽ��ũҵũ�壨ũ����������ҽ�������֡�ί�����½������������ũҵũ��֣� Ϊ������ֳҵ��Ʒ������ȫˮƽ���ӿ��ƽ�����ҵ��ɫ��չ�����ݡ�ũ��Ʒ������ȫ���������Ϻ��������Ӽ���������������ҩ��������������Ʒ������ȫ�ල�����������ȷ��ɷ���涨���Ҳ��ƶ��ˡ�2020��ȫ������������ȫ�ල���ƻ�����2020�궯�P�����Ʒ��ҩ������ؼƻ�����2020�궯��Դϸ����ҩ�Լ��ƻ�����2020��������������ȫ���ƻ�������ӡ�������ǣ�������ִ�С� ������1.2020��ȫ������������ȫ�ල���ƻ� 2.2020�궯�P�����Ʒ��ҩ������ؼƻ� 3.2020�궯��Դϸ����ҩ�Լ��ƻ� 4.2020��������������ȫ���ƻ�
ũҵũ�岿
2020��2��11�� ����1
2020��ȫ������������ȫ�ල���ƻ�
Ϊ��ʵǿ������������ȫ��ܣ��Ҳ�������ҽ�ְ���“˫�����һ����”��Ҫ��ȡ“������+���ϼ��”�ķ�ʽ����֯��չ2020��ȫ������������ȫ�ල��鹤�������ƶ��ල���ƻ����¡�һ�������ƻ� ��һ��ȫ������������ȫ�ල��� ȫ������������ȫ�ල��鹤�����ϰ�����°���2�ν��У��ֱ���2020��7��10�պ�11��10��ǰ��ɡ� 1.������ҵ�ල��顣��ȫ������������ҵ��¼�������ѡȡ1000����������������ҵ�������Ʒ3000�������ϡ� 2.������ҵ�ֳ���顣�ڱ��ල�����ҵ��ȷ��300�ҿ�չ������������ȫ�����淶��ִ�������顣 3.����Ԥ����⡣����������Ӫ��ʹ�û��ڿ�չ�����зǷ�������Ԥ����⣬�ص��Ʒ����������������Ӽ���ֲ����ȡ�ֲ��������ԭ�ϡ������Ƽ���ø�Ƽ��ͳ������ϵȡ���չ��������Ʒ������������ĺϹ��Ե���Ͱ�ȫ�Է��շ����� ������ʡ������������ȫ�ල��� ��ʡ�����Ϲ������Ÿ���Ͻ��������������ȫ�ල��鹤�����ල�������������ҵ����������Ͻ������ҵ������30%����ʡ�ݼල���������������1—1�������Ͻ�������Ͼ�Ӫ�ŵ꿪չ�ල��顣 ������������ ��һ��ȷ�����ල�����ҵ���Ҳ�������ҽ�ְ���“˫���”ԭ��ͨ��ȫ������������ȫ�����Ϣϵͳȷ��ȫ�����ල�����ҵ������ÿ��ʡ�����������ڸ�ʡ��ҵ������15%��2019�����Ҳ��ල����з��ֲ�Ʒ���ϸ����ҵ�ؼ졣 �������������⡣�������������ල�������ģ������������ȫ������������ȫ���ר�ҿ������ѡȡ100����Ա����ɹ����鸰���ල�����ҵ�ɼ���Ʒ����������м�����ɷ������Ʒ�����ڼල�����Ʒ�����Ϊ���ϸ�ģ����м����Ҫ�ڳ������ⱨ���48Сʱ�ڣ��Լij��ʴ�ʱ��Ϊ�����������ϸ���֪ͨ������������1—2���ͼ����ⱨ��ͨ�������ؿ�ר�ݼĸ����ල�����ҵ�������������ල�������ģ��������������ϸ���֪ͨ����ͬʱ�������Ҳ�������ҽ�֡���Ʒ�ɼ����������¼��������������ϢҪ��ʱ¼��ȫ������������ȫ�����Ϣϵͳ������Ҫ�����Ҳ�������������ȫ�ල������Ҫ��ũ������2019��22�ţ�ִ�С� ���������˼����ٲü��顣���ල�����ҵ�Լ�����������ģ������յ�������֮����5�������Ҳ�������ҽ���������븴�˼�⣨��ʽ������1—3�����������������ල�������ģ������������ɷ�������Ʒ���й�ʡ�������ʼ���������⣬����������Ҳ�������������ȫ�ල������Ҫ��ִ�У��������ɹ������������ල�������ģ���������֪���븴����ҵ����������������������ı��ල�����ҵ�е��� ��������Ҫ�� ��һ����ǿЭͬ��ϡ���ʡ�����Ϲ������ź��ʼ����Ҫ�߶����ӣ��������ȫ������������ȫ�ල��鹤������Ͻ���ڿ�չ����ع����� ��������ʱ����ʡ�����ƻ�����ʡ�����Ϲ�������Ҫ��2020��4��20��ǰ������ʡ���ල���ƻ������Ҳ�������ҽ�֣������������������ල�������ģ��������� ��������Ա�μ���ѵ�����м����Ҫѡ����Ա�μ��Ҳ�������ҽ����֯�������ѵ����ʡ�����Ϲ�������Ҫ֧�ֱ�ʡ����ȫ������������ȫ���ר�ҿ����Ա�μ��Ҳ�������ҽ����֯�������ѵ�� ���ģ����ϼ���������Ҳ�������ҽ��ί�й������������ල�������ģ��������Գм�����IJ�����Ʒ���м�������ˣ���֯��չʵ���Ҽ�������ȶԺͼ��������ֳ���顣 ���壩��������鴦����ʡũҵũ���������ܲ���Ҫ��ִ֯�������Բ��ϸ��Ʒ��������ҵ���е��飬�������в鴦������2020��12��31��ǰ��ȫ��鴦��������Ҳ�������ҽ�֡� �ġ���ϵ��ʽ ũҵũ�岿������ҽ�������Dzݴ� ��ϵ�绰��010—59191800��59192848�����棩 �����ʼ���xmjslch@agri.gov.cn ͨѶ��ַ�������г�����ũչ����11�� �������������ල�������ģ������� ��ϵ�绰��010—82106583��82106580�����棩 �����ʼ���gjzx@caas.cn ͨѶ��ַ�������к������йش��ϴ��12�� ������1—1.2020��ʡ������������ȫ�ල������� 1—2.���ϸ���֪ͨ�� 1—3.��Ʒ���ϸ����������뺯����ʽ�� 1—4.����Ԥ���������� 1—5.��ⷽ�� �ж����� �ж�ԭ�� ����1—1 2020��ʡ������������ȫ�ල�������
���ϸ���֪ͨ�� �����ල�����ҵ���ƣ��� ����ũҵũ�岿��2020��ȫ������������ȫ�ල���ƻ���Ҫ���ҵ�λ��Ϊ�м�����������ල�����ҵ���ƣ����Ϊ _____��_____��Ʒ�����˼��顣���ϸ�����ⱨ�湲____�ݣ����Ϊ____�������飬�����յ�����֮����5�գ���ũҵũ�岿������ҽ������������˼�����루����ϸע����ϵ��ʽ��������ָ�겻���ܸ��˼�����롣 �м�������ƣ�____________________________________ ��ַ�� ___________________________________________ ��ϵ�ˣ�___________ �绰�����棩�� _______________ �ֻ���_____________ �������䣺 ________________ ���м�������£� �� �� �� ע����֪ͨ���ͼ����ⱨ��ͨ�������ؿ�ר�ݼĸ����ල�����ҵ�������������ල�������ģ���������ͬʱ���棨010—59192848�����Ҳ�������ҽ�֣����绰ȷ�ϣ�010—59191800���� ����1—3 ��Ʒ���ϸ����������뺯 ũҵũ�岿������ҽ�֣� �� �գ��� ����λ���ƣ��ӵ� ���м�������ƣ����͵ġ����ϸ���֪ͨ�����ͼ����ⱨ�档��������˼�����롣 ���ɣ�____________________________________ ���뵥λ���� �� �� �� �� ϵ �ˣ�_____________ ��ϵ�绰��_____________���ֻ����������룩 ����1—4 ����Ԥ���������� Ϊ��ʵǿ������������ȫ��ܣ��Ҳ�������ҽ�ֶ�ȫ��������������Ӫ��ʹ�û��ڵ��ص����ϲ�Ʒ��չ����Ԥ����⣬���������ش�DZ�ڷ������أ�Ϊʵʩ��Ч����ṩ֧�š� һ���������� Χ�ƻ�����������Ӽ���ֲ����ȡ�ֲ��������ԭ�ϡ������Ƽ���ø�Ƽ��ͳ������ϵ��ص��Ʒ�����ص㻷��������Եزɼ���Ʒ�����ɸ��δ֪���ʡ�Υ��Υ��ҩ��������ʵȷǷ����������������ȫ���ա���չ��������Ʒ������������ĺϹ��Ե���Ͱ�ȫ�Է��շ����� �����ص����� ��һ�������зǷ�������ɸ�������Ԥ����⡣��Ҫ���ָ��Ϊδ֪���ʡ�Υ��Υ��ҩ��ͽ������ʵȡ��ɹ������������ල�������ģ������������ƶ�������������֯ʵʩ���й�ũҵ��ѧԺ�����о���������ʡ��������֤���ġ��Ϻ��ж����߲�Ԥ���������ģ��Ϻ�����ҩ���ϼ���������㽭ʡ��ҩ���ϼ������ɽ��ʡ��������������������ʡ��ҩ���ϼ����������ʡ���ϼ�������й�ũҵ��ѧ��ѧԺ�ȵ�λ����ʵʩ�� ������������������Ӽ�����Ԥ����⡣��Ҫ���ָ��Ϊ���ɷֺ�����δ֪���ʡ�Υ��Υ��ҩ��ͽ������ʵȡ����й�ũҵ��ѧԺ�����о��������ƶ�������������֯ʵʩ���������������ල�������ģ����������Ϻ��ж����߲�Ԥ���������ģ��Ϻ�����ҩ���ϼ������������ʡ��ҩ���ϼ�������Ĵ�ʡ���Ϲ�����վ���ൺ��ũ��Ʒ������ȫ���ĵȵ�λ����ʵʩ�� ������ֲ����ȡ���ֲ��������ԭ�Ϸ���Ԥ����⡣��Ҫ���ָ��Ϊ���ɷֺ�����δ֪���ʡ�Υ��Υ��ҩ��ͽ������ʵȡ����й�ũҵ��ѧԺ�����о��������ƶ�������������֯ʵʩ���������������ල�������ģ��������������ũҵ��̬���������ũ��Ʒ����������ġ��Ϻ���ũҵ��ѧԺũ��Ʒ���������⼼���о���������ũҵ��ѧ�����������ѧ��������ҵ����ѧԺ�ȵ�λ����ʵʩ�� ���ģ��������ϲ�Ʒ����Ԥ����⡣��Ҫ���ָ��Ϊ�������ϱ�ǩ����Ҫ������ȫָ��ͷǷ���������㽭��ѧ���Ͽ�ѧ�о��������ƶ�������������֯ʵʩ��ȫ��������վ���й����Ϲ�ҵЭ�ᡢ�������������ල�������ģ����������й�ũҵ��ѧԺ�����о������й�ũҵ��ѧԺũ��Ʒ�ӹ��о��������������ϼ�����ȵ�λ����ʵʩ�� ���壩����������ϲ�Ʒ����Ԥ����⡣��չ���־���Ϲ��Ե��������;����²��ԡ���ҩ�ԡ������ԡ���л��ȫ�Ե�DZ�ڷ��շ��������й�ũҵ��ѧԺ�����о������������Ͽ������ҹ����о����ĸ����ƶ�������������֯ʵʩ��ȫ��������վ���й����Ϲ�ҵЭ�ᡢ�������������ල�������ģ����������й�ũҵ��ѧԺ����������ҽ�о���������ʡ��ҩ���ϼ���������ɹ�ũҵ��ѧ�����ϴ�ѧ���й��������ϲ�ҵ����ս�����˻�Ա��λ����������������ȫԤ����Ŀ���վ�ȵ�λ����ʵʩ�� �����������л�����Ⱦ�����Ԥ����⡣��Ҫ���ָ��Ϊ�־��Ի�����Ⱦ���еĶ��ȴ����������fӢ�Ͷ��ȴ�������ૡ����fӢ������������ж����Ȼ�ʯ���ȡ��й�ũҵ��ѧԺũҵ���������⼼���о������������������ල�������ģ������������ƶ�������������֯ʵʩ�� ���ߣ�����������ȫ����Ԥ����⼼��ƽ̨��������չ���ϼ�����ԭ����δ֪���ʡ�Υ��Υ��ҩ��������ʵȷǷ�������ĸ�ͨ��ɸ�鼰�ۺϲ�ѯ�ȶԷ����о����Ϻ��ж����߲�Ԥ���������ģ��Ϻ�����ҩ���ϼ���������й�ũҵ��ѧԺ�����о������������������ල�������ģ����������𡣹������ݲ�ͬ����ɸ���ķǷ�������ɸ�鹲���⣬��չ���ϼ�����ԭ���ж��ֻ�����Ⱦ��ɸ�鼼���о����ݼ����з����������������ල�������ģ����������𡣿�չ���������þ��־���������ۼ���ƽ̨�Ĺ����ͳ���ֲ����Ҫ�����Գɷּ�⼼�����������������о����й�ũҵ��ѧԺ�����о������� ��������Ҫ�� ��һ������Ԥ�������Ʒ��Դ����������������Ӫ��ʹ�û����Լ����罻��ƽ̨�ɼ��������Ʒ��ȫ����ʡ������������ȫ�ල��鹤���вɼ�����Ʒ��Ҳ����Ⱥ�ھٱ��Ŀ���������Ʒ�� ����������Ԥ�������Ʒ�ļ����ⱨ�治������λ���͡� �������������Ԥ�����������λҪ��ʱ���Ҳ�������ҽ�ֱ��湤�������з��ֵķ�������������֯ר�Ҽ�ʱ����������ȫ���գ��������������� ���ģ�������ʵʩ��λ��2020��11��1��ǰ��ɳ����ͼ��������������̡��������������λ����������λ�γɹ����ܽᱨ�棬��2020��11��10��ǰ��ֽ���ļ��͵����ĵ������й�ũҵ��ѧԺ�����о������й�ũҵ��ѧԺ�����о�����2020��12��10��ǰ����2020��ȹ�������ܽᱨ�汨���Ҳ�������ҽ�֡� �ġ���ϵ��ʽ ũҵũ�岿������ҽ�������Dzݴ� ��ϵ�绰��010—59191800��59192848�����棩 �����ʼ���xmjslch@agri.gov.cn �й�ũҵ��ѧԺ�����о��� ��ϵ�绰��010—82106058��82106069/6059�����棩 �����ʼ���lijun08@caas.cn guxu@caas.cn ����1—5 ��ⷽ�� �ж����� �ж�ԭ�� ���ƻ����漰��ⷽ�����ж����ݺ��ж�ԭ�����¡� һ����ⷽ�� GB 5009.227—2016 ʳƷ��ȫ���ұ� ʳƷ�й�����ֵ�IJⶨ GB 5009.229—2016 ʳƷ��ȫ���ұ� ʳƷ����۵IJⶨ GB/T 5532—2008 ��ֲ����֬��ֵ�IJⶨ GB/T 6432—2018 �����дֵ��IJⶨ ���϶����� GB/T 6435—2014 ������ˮ�ֵIJⶨ GB/T 6436—2018 �����иƵIJⶨ GB/T 6437—2018 ���������IJⶨ �ֹ��ȷ� GB/T 8381.7—2009 ��������Ҵ��IJⶨ ��ЧҺ��ɫ��������1���ĵ��� GB/T 8381.9—2005 ��������ù�صIJⶨ ����ɫ�� GB/T 21108—2007 ��������ù�صIJⶨ ��ЧҺ��ɫ�״������� GB/T 13079—2006 ����������IJⶨ GB/T 13080—2018 ������Ǧ�IJⶨ ԭ�����չ��� GB/T 13082—1991 �������ӵIJⶨ���� GB/T 13088—2006 �����и��IJⶨ GB/T 13091—2018 ������ɳ���Ͼ��IJⶨ GB/T 13885—2017 ���������иơ�ͭ������þ���̡��ء��ƺ�п�����IJⶨ ԭ�����չ��� GB/T 14701—2019 ������ά����B2�IJⶨ GB/T 14702—2018 ���Ӽ�Ԥ���������ά����B6�IJⶨ ��ЧҺ��ɫ�� GB/T 17817—2010 ������ά����A�IJⶨ ��ЧҺ��ɫ�� GB/T 17812—2008 ������ά����E�IJⶨ ��ЧҺ��ɫ�� GB/T 17818—2010 ������ά����D3�IJⶨ ��ЧҺ��ɫ�� GB/T 18246—2000 �����а�����IJⶨ��2020��7��1��ǰ���ã� GB/T 18246—2019 �����а�����IJⶨ��2020��7��1�պ����ã� GB/T 19164—2003 ��ۣ���¼A�����ɰ�ֵIJⶨ������ GB/T 19684—2005 �����н�ù�صIJⶨ ��ЧҺ��ɫ�� GB/T 20190—2006 ������ţ��Դ�ԳɷֵĶ��Լ�� ���Ծۺ�ø��ʽ��Ӧ��PCR���� GB/T 22259—2008 ��������ù�صIJⶨ ��ЧҺ��ɫ�� GB/T 23710—2009 ��������˼�IJⶨ ����ɫ�� GB/T 30956—2014 ����������ѩ��������ϩ���IJⶨ ������������—��ЧҺ��ɫ�� GB/T 30957—2014 ����������ù����A�IJⶨ ������������—��ЧҺ��ɫ�� ũҵ��1486�Ź���—8—2010 �������������ҩ��IJⶨ ��ЧҺ��ɫ�� ũҵ��1629�Ź���—1—2011 ������16��β—���弤�����IJⶨ Һ��ɫ��—�������� ũҵ��2086�Ź���—5—2014 �����п�������������ୡ��ϩͪ����Ҵ��IJⶨ Һ��ɫ��—�������� ũҵ��2483�Ź���—8—2016 ��������ù�ء�����ù�غͷ����ῼ�IJⶨ Һ��ɫ��—�������� NY/T 1372—2007 �����������谷�IJⶨ NY/T 1946—2010 ������ţ��Դ�Գɷּ�� ʵʱӫ��ۺ�ø����Ӧ�� NY/T 1970—2010 �����з������صIJⶨ NY/T 2071—2011 �����л���ù���ء����׳�ùϩͪ��T—2���صIJⶨ Һ��ɫ��—�������� NY/T 3144—2017 ����ԭ��ѪҺ��Ʒ��18��β—���弤�����IJⶨ Һ��ɫ��—�������� NY/T 3145—2017 ������22��β—���弤�����IJⶨ Һ��ɫ��—�������� �������Ӽ��������ļ�ⷽ����������Ӧ�������Ӽ���Ʒ���й涨���Ƽ��ļ�ⷽ���� �����ж����� ��һ������ָ�ꡣ���ա���������������GB 13078-2017���ж����������Ӽ���Ʒ����������ҵ��Ʒִ�б��ж��� ����������ָ�ꡣ����������ҵ��Ʒִ�б�����Ч��ͬ����ʾָ�꣨���ϱ�ǩ����ʾָ�ꡢ��Ʒ˵���������ж�����������ҵ��Ʒִ�б�����ʾָ�ꡢ���������Ӽ���ȫʹ�ù淶����ũҵ�������2625�ţ���һ�£������н��ϸ�ָ������ж��� ������ҩ���������Ӽ��ͷǷ�����������Ϻ��������Ӽ���������������ҩ��������������ֹ�����ϺͶ�����ˮ��ʹ�õ�ҩ��Ʒ��Ŀ¼����ũҵ�������176�ţ�������ֹ�����ϺͶ�����ˮ��ʹ�õ����ʡ���ũҵ�������1519�ţ���������ֹͣ���������ڡ���Ӫ��ʹ�ò���ҩ���������Ӽ��Ĺ��桷��ũҵũ�岿�����194�ţ��������������ҩ��Ʒ�������������ĺű���Ĺ��桷��ũҵũ�岿�����246�ţ�����ʳƷ�����н�ֹʹ�õ�ҩƷ�������������嵥����ũҵũ�岿�����250�ţ���������ԭ�Ϻ����ϲ�Ʒ�������谷����ֵ�Ĺ涨����ũҵ�������1218�ţ��� ���ģ����Ϻ��������Ӽ���Ʒ��ǩ�з�����ֵ֤֮���ָ���ж������Dz�Ʒ�ı����ڡ� �����ж�ԭ�� ��һ������ָ���ж������ϲ�Ʒ�ĸ�������ָ�꼰������ָ�����ݡ����ϼ�����ж�����������GB/T 18823—2010��ִ�С� 1.�������Ӽ����ж�����������ָ�꼰������ָ�겻���Ƿ����� 2.ҩ���������Ӽ��ж�������2020��7��1��֮ǰ���������ϲ�Ʒ���ڹ涨��Χ��ʹ�õ�ҩ���������Ӽ�������������ʺ�Ľ�������ж��������涨�������ģ��ж�Ϊ���ϸ��ڳ���Χʹ�õ�ҩ���������Ӽ����Լ�ⷽ���Ķ�������ͼ��Ũ��Ϊ�ж��ޣ������ж����ж�Ϊ���ϸ���2020��7��1��֮�����������ϲ�Ʒ�е�ҩ���������Ӽ���ȷ�ϼ�ⷽ���ж������Զ�����Ϊ�ж��ޣ������������ж�Ϊ���ϸ�û�ж����ģ��Լ��������Ϊ�ж��ޣ���������ޣ�����ޣ����ж�Ϊ���ϸ� 3.�Ƿ���������ж���ȷ�ϼ�ⷽ���ж������Զ�����Ϊ�ж��ޣ������������ж�Ϊ���ϸ�û�ж����ģ��Լ��������Ϊ�ж��ޣ�����������ж�Ϊ���ϸ������谷���ж����ա�����ԭ�Ϻ����ϲ�Ʒ�������谷����ֵ�Ĺ涨����ũҵ�������1218�ţ��ж��� 4.ţ��Դ�Գɷ��ж���ţԴ�Գɷ֡���Դ�Գɷ���һ��Ϊ���ԣ�����0.25%�ļ���ޣ������ж�����ƷΪ���ϸ�ʹ��ʵʱӫ��PCR����ʱ������0.25%�����Զ���������ʵ��Ctֵ�������Ի������ж��� ��������Ʒ�ۺ��ж���һ��ָ�겻�ϸ��ж������β�Ʒ���ϸ�ˮ�ֽ�������ʹ�ã��������ۺ��ж��� ����2
2020�궯�P�����Ʒ��ҩ������ؼƻ�
Ϊ��ǿ��ҩ������أ��ٽ���ֳ���ڿ�ѧ��ȫ������ҩ�����϶���Դ��ʳƷ��ȫ���Ҳ�������ҽ���ƶ��ˡ�2020�궯�P�����Ʒ��ҩ������ؼƻ��������¼�ơ���ؼƻ��������¡�һ����֯ʵʩ �Ҳ�������ҽ�ָ���ȫ�����P�����Ʒ��ҩ������ؼƻ�����֯ʵʩ��������ʡ����ҽ�����������Ÿ�����֯��չϽ�����ݲ�Ʒ��ҩ������ع������������ɹ��Ҽ�ؼƻ���ͬʱ��Ӧ�ƶ�����֯ʵʩϽ����ҩ������ؼƻ�������������õ��ڹ��Ҽƻ���20%�������й���ҵ��λ���ɳн������������IJ���ʡ����ҩ��������͵����������������ա���ؼƻ����е���ؼ������ �������Ҫ�� ��һ����ʡ����ҽ��������������֯����Ͻ�������ݼ����Ʒ�������������Źٷ�ȡ����Ա���в��������ڳ�������ǩ�֡��е��������Ļ���Ӧ֧����Ʒ�������ط��ã���ٷ�������Ա������Ʒ�������������ɸ�����Ҫ��Ա�������ֳ�Э���ٷ�ȡ����Ա������ ����������ϸ�ִ�С��ٷ�ȡ�����͡�2020�궯�P�����Ʒ��ҩ���������ͼ�⼼������Ҫ�㡷�����¼�ơ�����Ҫ�㡷��������Ҫ���������Ϣ�� ���������ݲ�Ʒ��Ʒԭ����Ӧ�Ӷ�����ֳ�������ڳ�ȡ��ţ����Ʒ����ţ��ֳ�����������������չ�վ��ȡ����չ���⡢�����Լ�������Υ����ҩ���ģ�����ֳ����ȡ����Ʒ����Ӧ������������������֮һ�� ���ģ���ѧȷ��������ʽ����������ʱ�Σ�6�µ�ǰΪ��һʱ�Σ�7����10��Ϊ�ڶ�ʱ�Σ������ȳ�����������ijһʱ�μ��г��������������ٳ����⣬��Ӧ��ͬһ�������ظ������� ���壩��ҩ������ⰴ�ա�2020��ȶ��P�����Ʒ��ҩ������ⷽ��������������ִ�У�ȷ֤��������ʳƷ��ȫ���ұ����Ҳ�������ָ���ķ��������չ��ʹ��ϵķ���ִ�С����������������Ա����ⷽ���ͼ���ޡ�ȷ��������ƻ�ȷ���ļ���ޡ���ⷽ���ģ�Ӧ������ȫ����ҩ��������ҩ�Կ���ר��ίԱ��칫�ң����¼�Ʋ����죩�ύ������ϣ��������ٽ��м�⡣ �����������ѷ�����ȷ֤��������ɸѡ������������������������Ʒ��Ӧ��һ������ȷ֤��⣬��ȷ֤�������Ϊ�ϱ����ݡ� ���ߣ���������Ҫ�ϸ�ִ�м���������ƶȣ���Ҫ�����������ܱ��� ���ˣ���������Ҫ�ϸ�ִ�����ԣ����꣩��Ʒ�����ƶȡ��ڼ���������Ʒ���10���������ڽ���ⱨ���ͳ�����λ���ٷ�ȡ����Ա���ڵ�λ�������ڵ����ؼ�ʡ��������ҽ�����������š�ʡ��������ҽ�����������ż�ʱ�����������ٳ�����������������Ϊ1:5����ÿ����һ��������Ʒ���Ա�������λ�������ٳ���2�Σ�ÿ��5����Ʒ���������ٳ��������Ʒ������Ͻ��������ؼƻ�����ý����Ҫ������� ����������� ����Ҫ��һ��ǿ�����������Ʒ�ĺ���������ʡ����ҽ������������Ҫ���ø��ٶ��죬��Ʒ��Դ���ڵ���ҽ�����������Žӵ������������IJ��������ⱨ������л��������P����ԴʳƷ�в������ʼ�ؼƻ�����ũ������1999��8�ţ������ݳ��� ��һ�����ݲ���������Ʒ������Ϣ��Դ������ֳ��������ֳ����ҩ������к˲飬�ص�����ҽ��������ҩ��¼�Ϳ����ҩ��Ʒ�� ������������ֳ��ҩ���淶��δִ����ҩ�ڵ�����Ҫ��ʱ���������ʩ�����ල���ġ����ݡ���ҩ�����������йع涨����ʹ���˽���ҩ�P����������Ķ��P���ƷҪ�ල��ֳ����������ҵ�������������� ���������ּ��ӡ�����ҩ�P����������Ҫ������٣���ʱ���汾��ʡ����ҽ�����������ţ�ͬʱͨ�������ҩ������ҵ���ڵ�ʡ����ҽ�����������ţ���������鴦Υ��Υ����Ϊ���Է���ũҵũ�岿�����97�Ŵ��ش��������Σ�Ӧ�����������ҩ������ҵ����Ӫ��ҵ���Դ��ش����� ���ģ�����������Ʒ�������Ҫ��ʱ��ʡ��������ҽ�����������ţ������õ��鴦����¼����¼�浵2�����ϡ� �ġ�����Ҫ�� ��һ���е������ͼ������ĵ�λҪ������ϣ���ʱ��ͨ��������ա�����Ҫ�㡷��ɼ����Ʒ�ij������Ǽǡ����桢���Ӻͼ����� �������е��������λ��2020��7��15�պ�11�� 15��ǰ������������������ر����ֽ�ʲ��Ϻ͵��Ӱ�ִα������졣 �����������츺����ҩ������������ܺͼ�ؼƻ�ִ��������ܽ��ϱ����������Թ����ܽ��ȫ�깤���ܽ�ֱ���2020��7��31�պ�12��10��ǰ���Ҳ�������ҽ�֡� ���ģ��Ҳ��������ݼ����ݲ�Ʒ�����Ʒ��ҩ��������������ͨ�������Լ�ʱ���ͼ�������Բ���������Ʒ��չ�����Դ�����ʡ��ͨ����� ���壩����Ҫ�������д��ڵ�����ͽ��鼰ʱ�����Ҳ�������ҽ�ֺͲ����졣 ������2–1.2020�궯�P�����Ʒ��ҩ������ؼƻ� 2–2.2020�궯�P�����Ʒ��ҩ������ؼƻ���ʡ������ֹ��� 2–3.2020�궯�P�����Ʒ��ҩ���������ͼ�⼼������Ҫ�� 2–4.2020�궯�P�����Ʒ�����������������ټ�������ܱ� 2–5.2020��ȶ��P�����Ʒ��ҩ������ⷽ������������ ���� 2–1 2020 �궯�P�����Ʒ��ҩ������ؼƻ� 1. ���ݲ�Ʒ����
2.���Ʒ����
2020 �궯�P�����Ʒ��ҩ������ؼƻ���ʡ������ֹ���
���� 2–3 2020 �궯�P�����Ʒ��ҩ���������ͼ�⼼������Ҫ�� 1.2020�������ؼƻ���Ϊ2��ʱ��ִ�У�6�µ�ǰΪ��һʱ�Σ�7����10�µ�Ϊ�ڶ�ʱ�Ρ�Ҫ�ϸ�ִ�б�ʱ�γ�������ʱ�μ�������Ҫ���ò�ȡȫ���ؼƻ�������һ��ʱ����ɻ�һ�γ��������л��ʱ�μ��������� 2.��ؼƻ��������������Ʒ�ֱ��밴���´�ļƻ�ִ�С� 3.�����취 3.1���ݲ�Ʒ���� 3.1.1��ֳ�������������������̣� 3.1.1.1���ݶ���������������������������м�����������Һ�л�������ģ���������������֮һ����Ʒ��Դ����ֳ���� ������ ������������������������������ <500 3 501–1000 7 1001–5000 10 5001–10000 12 >10000 15 ţ�� ������������������ ������������ <50 5 51–100 8 101–500 12 >500 15 ���ݣ����� ������������������ֻ�� ������������ <1000 1 1001–5000 3 5001–10000 5 >10000 8 3.1.1.2һ����Ʒ����ɼ�ȡ�������� �ռ��峿��ιǰ����Һ 100–200 ml�� ������Ʒ �����Ӳ������ϳ�ȡ��ȡ���������� 10 ö�� �̣���ȫ���������ȡ��ȡ���������� 1000 ml�� 3.1.2���׳�������������֯�� 3.1.2.1��������������������������� ����������ţ�� ����������������ͷ�� ������������ <100 5 101–500 8 501–2000 10 >2000 15 ���ݣ����� ����������������ֻ�� ������������ <1000 1 1001–5000 3 5001–10000 5 >10000 8 3.1.2.2һ����֯��Ʒ��������±�
3.1.4��Ʒ�ָ������Ҫ���ɹٷ���ҽ��Ա��ٷ���ҽ��ԱЭ���������������Ա���ֳ�����Ʒ�ֳ����ݣ�һ���ͼ죬һ���ɱ�������λ���档 3.1.5��Ʒ��װ��������������ϴ���װ���⸽��ǩ���������Ϻ��ں��ý����ܷ⣬�ں������ϳ����������������ϴ��ܷ⣨��ǩ�ͳ�������Ӧ���涨������д�����Ӹdz�����λ���£�����Ʒ��װ�� ��ǩ�ͷ���Ҫͳһ�� 3.1.6��Ʒ���棺ȡ��������Ӧ��ȡ���±����ʩ��ȡ����Ӧ��������Ʒ����-20°C ���±��档 3.1.7����������Ʒ�з���ɾ���������Ӳֽ���䡢������ĭ�䣩 ���ܷ�װ�ˣ�����ȡ���´�ʩ���¶ȿ����� 0–5°C������д������һ���ͼ졣 3.2 ���۳��������Ʒ�����ɼ�ⵥλ�е���70%��Ʒ�ӷ��ۼӹ�����ȡ��30%��Ʒ�ӷ䳡��ȡ��ÿ����Ʒ��Ϊ 1000 �ˡ�����ʱ���ɳе��������λ���ݷ����������ȷ������Ʒ��ת������ձ��취ִ�С� 4.��������д˵�� ��Ʒ��ţ���ʽΪ[����Ʒ�ִ���]/[��Ʒ�������]/[��������]�� �������£�
��Ʒ���ƣ���ȡ��Ʒ�����༰��λ������ȫ�Σ�������ȡ� ����Ʒ�֣���ȡ��Ʒ��������ơ� �� �䣺ţ������ƣ������¼ƣ������ռơ� ������������������ij����ʣ���ֳ�����������������׳��������������⣩�� ������������ȡ��Ʒ������������� �� �ţ���Ʒ�����������ţ����ޣ�����“��”�� �������������ǰ����ȡ�ı��淽ʽ�������¶ȼ�����ʱ�䡣��װ�������Ʒ����������������õĴ�������װ�� ��������������õ���Ʒ���䷽ʽ����������е��¶ȼ�����ʱ�䡣 5.��������д˵�� ��������ţ��ɼ��������ݱ���λ���������س�����������ţ�һ����Ʒһ������������Ÿ�ʽΪ[��������ǰ 4 λ]��������ţ� �籱�� 2018 �� 8 �� 10 ���ͳ��ĵ� 6 �����������������Ϊ[1000]2018/08/10/06�� ��Ʒ��ţ�ͬ�������еı�š���Ʒ���ƣ�ͬ�������е����ݡ� ��Ʒ��������ȡ��Ʒ������������� ���������ָ��װ������Ʒ�õ��������С����ϴ��������������ͬ�������е����ݡ� ���������ͬ�������е����ݡ� ������Ŀ��ָҪ��������ҩ��Ʒ�֡� 6.��Ʒ��ת���� 6.1ȡ����Ա��ȡ��Ʒ������ȡ��Ʒ�ֳ� 2 �ݣ�1 ����Ʒ����������λ���棬1����Ʒ�ͼ죬����д������һʽ���ݣ��ٷ�ȡ����Ա�ڳ�������ǩ�ֱֺ��ɼ���������������λ�����������棩�ٷ�ȡ����Ա���ڵ�λ���档 6.2���г���������Ʒ�ɼ�����������Ա���ؼ������� 6.3�������ҵ�����������������д��Ʒ��ⵥ��������Ʒ���ٽ���Ʒ���±���ͼ����Ҽ��飨�������������������������Ҹ����˰��ż�⣬����ԱӦ�ڽ����� 15 ������ɼ�⣬����д�����¼��������˫ä����������Ա����֪����Ʒ����Դ�غ���Ʒ��š� 6.4�����ҳ���ԭʼ���浽�������ҵ��������ţ��ɼ������ҵ����������������������ܱ����������졣 7.�������ִ��ʳƷ��ȫ���ұ������ұ��ģ�ִ���Ҳ�������ָ���ķ�������ʹ��ϵķ����� 8.��⼼�������Ŀ��ˣ��ڼ����Ʒ֮ǰһ��Ҫ���м��������������顣��귨Ҫ���б����ߣ�һ��Ҫ�� 5–6 ��Ũ�ȣ�����Ҫ���� 1/2MRL��MRL��2MRL�������������飨���� 1/2MRL��MRL��2MRL3 ��Ũ�ȣ��ͱ���ϵ���ⶨ��һ��Ҫ�ظ� 3–5 �λ��������飩���õ��ڱ������Ҳ��������µĸ���������Ժ����ʱֻ�� 1 ���������ӽ��п��켴�ɡ����в���������ҩ���ڼ�������ʱ��Ҫ��ƽ�����������㣨�����ʵ���һ�õ�ƽ�������ʣ������ڽ���ҩ�������㡣�ڱ귨ҲҪ���л����ʺͱ���ϵ�����졣���ʱ�����������Ժ��������Ӷ����顣 9.��ⱨ���ƶ� 9.1����Ա��������ҵ��������ų���ÿһ����Ʒ�ļ��鱨�棬 ��Ӧ�����������㷽���� 9.2�������Ӧ��������������������ͼ��������ܱ����ƹ��������м������������Ӧ����������ҩ������ؼƻ���Ͻ���ƻ�ִ�����������������Ʒ��Դ��������������ͽ���ȡ����������ܱ� “�����”һ��Ӧ��������д��ʽ��δ����ģ����ڼ���ޣ����� ND ��ʾ������������ʵģ�����д���������ݡ����������һ�ɲ��� A4 ֽ���Ŵ�ӡ�� 9.3������Խ�������� 10 ���������ڱ��ͱ�������λ����ʡ������ҽ�����������źͲ����죬�ɱ�������λ����ʡ������ҽ��������������֯���ٵ��鴦����������鴦������豨�����챸���� 9.4����������ͼ�������ܱ�ֽ�ʲ��Ϻ͵��Ӽ������α������졣 ���� 2–4 2020 �궯�P�����Ʒ�����������������ټ�������ܱ� ��һ ��ҩ������ؼƻ�����������ܱ���2020 ��ȵ�×ʱ�Σ�
���� ��ҩ������ؼƻ���������ܱ���2020 ��ȵ�×ʱ�Σ�
���� ��ҩ������ؼƻ�������Ʒ�ټ�������ܱ���2020 ��ȵ�×ʱ�Σ�
���� 2–5
��ҩ������ⷽ������������
1. ���ݲ�Ʒ����
2. ���Ʒ����
����3
2020�궯��Դϸ����ҩ�Լ��ƻ�
���ݡ�����ϸ����ҩ�����ж��ƻ���2016-2020�꣩����ȫ�����ƶ���Դϸ����ҩ�ж��ƻ���2017—2020�꣩�������Ҫ��Ϊ����2020�궯��Դϸ����ҩ�Լ�������ַ��Ӽ�����֧�����ã��ٽ���ֳ���ڿ�ѧ������ҩ���ƶ����ƻ���һ������ֹ� ��һ��ũҵũ�岿������ҽ�ָ�����֯��չȫ������Դϸ����ҩ�Լ������ƶ��������ƻ���������Ӧ�ü������ �������й���ҽҩƷ����������¼���м���������ȫ������Դϸ����ҩ�Լ����ļ���ָ�������ݿ⽨����ά��������ҩ��������������������ơ�������Ļ��ܺͷ����� ������ʡ����ҽ�����������Ÿ���������ȫ������Դϸ����ҩ�Լ����������Э������е���λ���ö������׳�����ֳ���IJ���������������ʡ��Ӧ�������ż�⾭�ѣ��ƶ�����֯ʵʩ��Ͻ������Դϸ����ҩ�Լ��ƻ��� ���ģ��������е���λ��Ҫ�����ȫ������Դϸ����ҩ�Լ����ƻ����������������3—1�� ���壩�����걣���������λ�У��м�������Ը�����ҩ�Լ������е���λ�����������ԭ����ɳ���Ͼ��ͽ��ɫ������������ֵı��棬��ָ��������е���λ����ɳ���Ͼ�Ѫ����ͣ�ɳ���Ͼ�������ҩ���;����ȷ�ϡ��ռ��ͱ����Լ���ҩ���Ƶļ������й�ũҵ��ѧ��������������˾�������ҩ���;����ȷ�ϡ��ռ��ͱ����Լ���ҩ���Ƶļ���������ũҵ��ѧ����˾�������ҩ���;����ȷ�ϡ��ռ��ͱ����Լ���ҩ���Ƶļ���������ũҵ��ѧ��������Ѫ�˾���κ�����������ҩ���;����ȷ�ϡ��ռ��ͱ����Լ���ҩ���Ƶļ���������ũ�ֿƼ���ѧ����α��˰�״�˾�������ҩ���;����ȷ�ϡ��ռ��ͱ����Լ���ҩ���Ƶļ����� ������ⷶΧ��ԭ�� ����Դϸ����ҩ�Լ�����dz��������30��ʡ�������У���ʵ�ж���������������ϡ�2020��������2019��ȫ�����ÿ���ҩʹ�ü������ж��Ե���ֳ����Ŀ¼������3—2����Ϊ�����ⳡ����Ҫ��������ټ��2018��ȫ�����ÿ���ҩʹ�ü������ж��Ե���ֳ���ͼ�����г��ڶ��������ֳ�����������������������ڵ�����3�����У�ÿ������3����ֳ�������׳��� ��һ�����˾���ɳ���Ͼ�������Ѫ�˾���3�ָ��������Ծ��������֡���Ī����/����ά�ᡢ���ù�ء����ù�ء��Ļ��ء������ῼ���ǰ���f�������/�ǰ��ׇf��ͷ������ͷ����ड���ŵɳ�ǡ�����ɳ�ǡ��������ϡ�����ù�ء����ء��������16�ֿ���ҩ����ҩ�ԡ� ��������⳦��������ɫ���������κ�������α��˰�״�˾���4�ָ��������Ծ�����ù�ء���Ī����/����ά�ᡢ��ù�ء�����ù�ء���ŵɳ�ǡ�����ɳ�ǡ�ͷ������ͷ���������ǰ���f�������/�ǰ��ׇf�����ù�ء��������ء������ῼ���������֡����ù�ء�̩����ء������ǡ�������18�ֿ���ҩ����ҩ�ԡ� ��������������˾�����ù�ء�����ɳ�ǡ���ù�ء����ù�ء��Ļ��ء������ῼ������ᡢ̩��ù�ء�����ù��9�ֿ���ҩ����ҩ�ԡ� ���ģ���⳦�����κ��������Ļ��ء�����ù�ء���ù�ء�����ù�ء��ϩͪ�������ġ���ά��ù�ء�ά������ù�ء��˾���9�ֿ���ҩ����ҩ�ԡ� �������Ҫ�� ��һ�����������е���λҪ���ա�����Դϸ����ҩ�Լ������ͼ�⼼��Ҫ�㡷��������3—3����չ������ϸ������ͼ�������ҩ�Լ��ͽ���ϱ��ȹ����������ж�Ϊ���ù�ء�����������ҩ�ļ��������Ӧ�е���λ�ϱ��������֮ǰ�������Ӧ������ҩ�Լ�������и��ˡ� ��������ƷӦ����ֳ������������������Ѽ������������������ţ���������׳���ȡ������ֳ�������ģ���ģ����ģ���³���ռԼ50%�� ������������ͬʱ��Ӧ������ֳ����ҩ�����������Դ���飬������д��������¼������������3—4������ͬһ��ֳ����ҩ�����ͬ�Ķ���Ⱥ��Ӧ�ֿ���д�������� ���ģ�ϸ���ķ���ͼ������ա�����Դϸ������ͼ���������������3—5���������ع��ʱ�ִ�С� ���壩������е���λ����ҩ������ʱӦʹ�þ���������֤�ļ��塣2020�������⳦�����κ������Դ������ÿ���ҩ�����ҩ�ԡ�ҩ��������壨MIC�ⶨ��ʹ�÷���������3—6�� �ġ�������� ��һ����½�й���ҩ��Ϣ����www.ivdc.org.cn�������й���ҩ���ݿ���ѡ��“��ҩ��ҩ�Լ�����ݿ�ϵͳ”�����뱾��λ�û��������룬����ʵ������ظ��������ͨ������ҩ�Լ�������ϴ������ݿ⣬Ȼ������ܽ������ ��������������ֹ������������е���λ�ĵ��Ӱ��ܽ���2020��10��31��֮ǰ���м�����2021��1��31��ǰ�����м�����ɻ��ܷ������Ҳ�������ҽ�֡� ����3—1
2020�궯��Դϸ����ҩ�Լ��ƻ�
1.��ֳ��������Ҫ���Գ���ǰ������ڴ˾�������������ɫ��������������˾�����ͬ��ֳ�λ���ͬ�β�ͬȦ��ɼ�����Ʒ����õ��ľ��꣬����Ϊ��ͬ���ꣻ��ͬ����ͬȦ��ɼ��ľ�����Ϊͬһ���ꡣ����ɳ���Ͼ���ͬһ��ֳ��������5�꣨������Բ�ͬȦ���ͬ��ֳ�Σ��� 2.������Դ�漰����ֳ����ģҪ�����С����ֳ�����롣 3.���ݲ�ͬ���������Ͷ������࣬������������������䣬����ũҵũ�岿������2018�ꡢ2019��ȫ�����ÿ���ҩʹ�ü������ж��Ե���ֳ���� 4.���׳������У�����ͬһ��ֳ������ľ��겻����3�ꡣ ����3—2 ȫ��������ټ����ֳ����¼ ��2019��ȫ�����ÿ���ҩʹ�ü������ж��Ե���ֳ��������
����Դϸ����ҩ�Լ������ͼ�⼼��Ҫ�� һ���������� ��һ�������ص�ѡ�� ���������е���λ���ա����ƻ�������ѡ���������ͷ���ϸ����ͬʱ������Ա�ʡ��������ȫ�������ⳡ�����±������ڸ��ټ��˾��ͳ������ҩ�Ա仯���ơ� �������������� ��������ɼ��ٴ����Ϸ��붯�ﲡԭ������������ɼ�йֳǻ��ä�����ӷ���˾����������ɳ���Ͼ��������˾����ɼ�����ţ�̷�����ɫ���������������ֳ����ģ��ÿ��������30~50�ݡ� ����������ϸ������ �����˾������������Ϊʺ������ͷ೦�������ɳ���Ͼ������ɫ��������������˾�����Ϊ�ճ������˾��ͽ᳦�����˾�����κ�������α��˰�״�˾���������Ѫ�˾��ȡ�ɳ���Ͼ��ͽ��ɫ��������ɸ��ݸ��ط���������м�⡣ ��������ͼ�¼ ���������е���λҪ�����������Ϻ�����ҩ�����Ӽ���Դ��������顢����ǰ����ʹ�ÿ���ҩ��������飨Ԥ����ҩ��������ҩ���Ͳɼ���Ʒ��ͳ�ƣ���ʵ��д������¼���� ����ϸ����������� ����ѡ�������������������˾����������ɳ���Ͼ������ɫ��������������˾����룬���������顢PCR������Ѫ��ѧ�����Է�������м���������ȷ������ϸ������������Ҫ��������ƻ��������뵽�ľ�����-20�����¼Ӹ��ͱ������䶳��������������ʷ������б��棬ɳ���Ͼ��������˾����й���ҽҩƷ���������Ѫ���ͼ����档 �ġ�ҩ�������Բⶨ �þ��й���ҽҩƷ����������϶���ҩ����������ҩ�������Լ�⡣Ŀǰ�ѽ��������϶���ҩ����������ҵ�У�����н��¿Ƽ���չ����˾���Ϻ��ǰ����\������˾��������ʿؾ������й���ҽҩƷ�����ͳһ��Ӧ�� ����3—4
������¼��
�� �� �أ� �� ֳ ���� ����ʱ�䣺 ��ϵ���������绰��
����3—5 ����Դϸ������ͼ������� һ������Դ�˾��ķ������������ 1 ��Χ �������涨�����ڶ���Դ�˾�����������ķ����� �����������ڸ��ֶ����д˾��ķ���������� 2 �豸�Ͳ��� ������ʵ���ҳ�������������豸�⣬�����豸�Ͳ������¡� 2.1 ���䣺2�桫4���-20�档 2.2 ���������䣺36��±1�档 2.3 ������ƽ������0.1g�� 2.4 ������10×��100×�� 2.5 ���ﰲȫ�� 2.6 ��������������Ʒ����ֽ���� 2.7 �����ܻ���Ʒ�����������ӡ� 2.8 ����������1μL��1000μL�� 2.9 ��ͷ������������ƥ�䣩�� 3 ���������Լ� 3.1 ������������ 3.2 ����֬�� 3.3 �˾�����Ѫ�塣 4 �˾�������������� �˾���������������ͼ1��  ͼ1���˾�������������� 5 �������� 5.1 ���� ѡ����ֳ�������׳�����������Ӳɼ�������Ż�йֳǻ��Ʒ�����������������У�����ʱ�䲻����48Сʱ�� 5.2 �˾��ķ��� 5.2.1 ���ӽ���������֬ƽ�壬36±1������18��24h�� 5.2.2 ��ȡ�ۺ�ɫ����Ե�⻬�Ŀ��ɾ��䣬����֬����һ���� 5.2.3 ��������ɾ������Ӫ����֬ƽ�崿����36±1������16��18h������һ��ϸ�������� 5.3 �˾��ļ��� �����Ѵ����ľ��䣬��ʹ��������������ϵͳ�������������������������� ��Ҫʱ�����ô˾���Ѫ�����Ѫ���ͼ����� ��������Դɳ���Ͼ��ķ������������ 1��Χ �������涨�����ڶ���Դɳ���Ͼ�����������ķ����� �����������ڸ��ֶ�����ɳ���Ͼ��ķ���������� 2 �豸�Ͳ��� ������ʵ���ҳ�������������豸�⣬�����豸�Ͳ������¡� 2.1 ���䣺2�桫4���-20�档 2.2 ���������䣺36��±1���42��±1�档 2.3 ������ƽ������0.1g�� 2.4 ������10×��100×�� 2.5 ���ﰲȫ�� 2.6 ����ˮԡ����37�桫100�档 2.7 PCR�ǡ� 2.8 ��Ӿ�ǡ� 2.9 ��Ӿ�����������ϵͳ�����������ǣ��� 2.10 �䶳���Ļ��� 2.11 �����ܻ���Ʒ���������ӡ� 2.12 С�����Ĺܡ� 2.13 ����������1μL��1000μL�� 2.14 ��ͷ������������ƥ�䣩�� 2.15 �����ǡ� 2.16 ��¯�� 3 ���������Լ� 3.1 �����꣺ɳ���Ͼ�CVCC 541 3.2 DNA Maker 3.3 Taq DNA �ۺ�ø 3.4 dNTP 3.5 ��֬�� 3.6 5×TBE����Һ ���Ǽ��������飨Tris�� 54.0g ���� 27.5g 0.5M EDTA��pH8.0�� 20mL �Ӵ���ˮ�� 1000mL 3.7 50×TAE buffer ���Ǽ��������飨Tris�� 242g NA2EDTA.2H2O 37.2g ���� 57.1ml �Ӵ���ˮ�� 1000mL 3.8 invA�������� ����Ϊ5′-GTG AAA TTA TCG CCA CGT TCG GGC AA-3′ ����Ϊ5′-TCA TCG CAC CGT CAA AGG AAC C -3′ 3.9 ������������ 3.11 ɳ���Ͼ���ɫ��֬�� 3.12 ɳ���Ͼ�����Ѫ�塣 3.13 ���������װ�������Һ��SC���� 3.14 �������������Һ��TTB���� 3.15 ����Ⱦ�ϡ� 3.16 �Ȼ��ơ� 4 ɳ���Ͼ�������������� ɳ���Ͼ���������������ͼ2�� 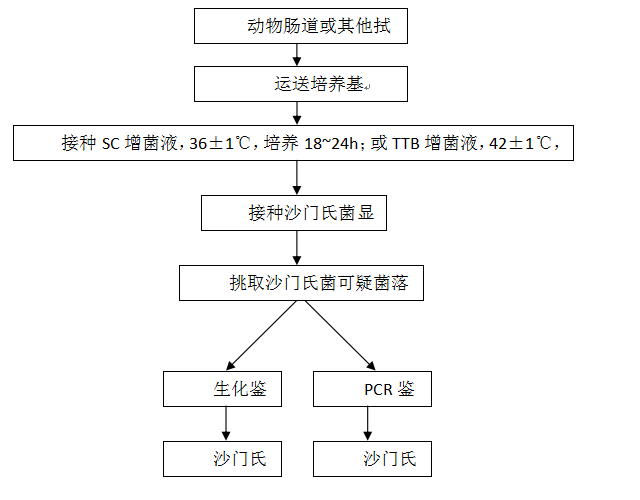 ͼ2 ɳ���Ͼ��ķ���ͼ������� 5 �������� 5.1 ���� ѡ����ֳ�������׳�������������Ӳɼ����ﳦ����йֳǻ�����ţ���Ʒ�����������������У�����ʱ�䲻����48Сʱ�� 5.2 ɳ���Ͼ��ķ��� 5.2.1 ����������SC����Һ��36��±1������18��24h ��TTB����Һ��42��±1������22��24h�� 5.2.2 ����Һ���ȣ�����ɳ���Ͼ���ɫ��������36��±1������22��24h�� 5.2.3 ��ȡɳ���Ͼ���ɫ����������ɫ���ɾ��䣬����Ӫ����֬ƽ�壬36��±1������16��24h������һ��ϸ�������� 5.3 ɳ���Ͼ��ļ��� 5.3.1 �������� �����Ѵ����ľ��䣬��ʹ��������������ϵͳ������������������������������ͨ��5.3.2�ķ������з�������ѧ��PCR�������� ��Ҫʱ����ɳ���Ͼ���Ѫ�����Ѫ���ͼ����� 5.3.2 PCR������ 5.3.2.1 PCRģ����Ʊ� �ý��ֻ���Ӫ����֬����ѡ16��24h�Ĵ����������0.5mL���������ˮ�У�12000r/min����2min�������塣�ټ�0.5mL���ˮ���������������ȣ�100���ˮ�����10min���������ϣ���ȴ����12000r/min����2min��ȡ����ҺΪPCRģ�塣 5.3.2.2 PCR��Ӧ��ϵ������ ���ݲ�ͬ����PCR�Լ�����������PCR��Ӧ��ϵ������Ƭ�γ���Լ284bp�� 5.3.2.3 PCR��Ӧ���� 95��Ԥ����5min��94�����30s, 64���˻�30s��72������30s, 30��ѭ�������72������10min��ͬʱ�������Ժ����Զ��ա� 5.3.2.4 ��Ӿ 5.3.2.4.1 1.2%��֬����������Ʊ� ��ȡ1.2g��֬�ǣ�����100mL0.5×TBE����1×TAE������Һ�У��������Ⱦ�ϣ�������Ʒ��ѡ�����˵����ӣ���֬���ܻ�����ȵ�����ˮƽ̨���ϵ��������У������5mm���ҡ���������ȴ���̺�γ����ӣ�ȡ����������Ӿ���У���0.5×TBE����1×TAE������Һ��û���档 5.3.2.4.2 ���� ȡ10µLPCR���������3µL��������Һ���Ⱥ��������ף�ÿ�ε�Ӿʱ������һ�����Զ��պ����Զ��ա� 5.3.2.4.3 ��Ӿ���� ��ѹ110V����Ӿʱ��30min�� 5.3.2.5 ����ж� ��Ӿ������ȡ��������������Ͷ�����ϴ�����ƹ۲�������������ǽ��г�������� ���ijһ������Ʒ���������������ɳ���Ͼ����Զ��յ�������һ��ֱ���ϣ�������������ľ�����ͬ�������Զ����������������Ʒ���뵽�ľ���ɳ����ж�Ϊɳ���Ͼ�����Ҫʱ��ͨ����������һ��ȷ֤�� ��������Դ���ɫ��������ķ������������ 1 ��Χ �����涨��������ҩ�Բⶨ�Ķ���Դ���ɫ��������ķ���ͼ��������� ����������ţ�̡�������֯���Ϻ������н��ɫ��������ķ���ͼ����� 2 �豸�Ͳ��� ������ʵ���ҳ�������������豸�⣬�����豸�Ͳ������£� 2.1 ���䣺0�桫4���-20�档 2.2 ���������䣺36��±1���42�档 2.3 ������10×��100×�� 2.4 ��Ʒ�������Ʋ����ܡ� 2.5 �����Ĺ� 2.6 ���Ļ��� 2.8 ��Ʒ����������������ǡ� 3 ���������Լ� 3.1 �����꣺���ɫ�������ATCC29213 3.2 ��ɫ������ 3.3 7.5%�Ȼ�������10%�Ȼ��������˴����� 3.4 Ӫ��������BHI���� 3.5 Ӫ����֬ 3.6 ������Ѫ������Ʒ������ø������Ѫ�� 3.7 0.3%��������Һ 3.8 0.85%��������ˮ 4 ���ɫ�����������ͼ������� ���ɫ�����������ͼ��������ͼ3��  ͼ3 ���ɫ�����������ͼ������� 5 �������� 5.1 ���� 5.1.1ţ����Ʒ������ѡ������ţ��ֳ�����ֳ���ţ����������Թ��У�0�桫4�汣�棬������48h�� 5.1.2�����塢����������֯���Ϻ��������ӣ�������ȡ����������֯���Ϻ��������ӣ��Ϻ�����������������Թ��У�0�桫4�汣�治����48h�� 5.1.3 ��ȡ1mLţ����Ʒ���Ϻ�����������ʢ��10mL 7.5%�Ȼ���������10 %�Ȼ��������˴������У����ȡ� 5.2 �����ͷ������� 5.2.1 ��������Ʒ��Һ��36��±1������18��24 h�����ɫ���������7.5%�Ȼ��������гʻ��������� 5.2.2 ������������ֱ��߽��ֵ���ɫ������ƽ���ϣ�������������������ֱ֯�ӻ��ߣ� 36��±1������24��48h�� 5.2.3 ��ȡ���ɾ��䡣��Ӫ����֬����һ��������һ��ϸ�������� 5.3 ���ɫ��������ļ��� 5.3.1�������� ����Ӫ����֬������24Сʱ���ڵĴ�����ϸ�������Ƚ��д�ø���飬ӦΪ���ԡ� �����ʴ���������ø�������Դ���ϸ���������䣬������5mL���������ˮ������������������ʹ��˵���������37������18��24h���ж������ 5.3.2Ѫ������ø���鷨 ��ȡ��ɫƽ���Ͽ��ɾ���1�������ϣ��ֱ���ֵ�5mL BHI��Ӫ����֬ƽ�壬36��±1������18��24h������Ӫ����֬������24h���ڵĴ�����ϸ�������Ƚ��д�ø���飬ӦΪ���ԡ� ������Ѫ���Ʊ�����ȡ��������3.8g��������ˮ100mL,�ܽ����ˣ�װƿ��121���ѹ���15min��ȡ3.8%����������Һһ�ݣ�����ȫѪ�ķݣ���þ��� (����3000r/min ����30 min)��ʹѪҺϸ���½������ɵ�Ѫ���� ȡ����������Ѫ��0.5 mL������С�Թ��У��ټ���BHI ������0.2��0.3 mL����ҡ�ȣ���36��±1�������ˮԡ���ڣ�ÿ��Сʱ�۲�һ�Σ��۲�6 h����������̣������Թ���б����ʱ���������飩�������������ԭ�����һ�룬���ж�Ϊ���Խ����ͬʱ��Ѫ������ø�������Ժ�����������������������������Ϊ���ա�Ҳ������Ʒ�����Լ�����˵�������������Ѫ������ø���顣 �ġ�����Դ�����˾��ķ������������ 1 ��Χ �����涨�˶���Դ�ճ��������ͽ᳦�������ķ������������ ���������ڷ�����Ӻ�ä���������пճ��������ͽ᳦�������ķ���������� 2 �豸�Ͳ��� ������ʵ���ҳ�������������豸�⣬�����豸�Ͳ������¡� 2.1 ������ 2.2 ���������� 2.3 ���ﰲȫ�� 2.4 ����������: 25��±1�棬36��±1�棬42��±1�档 2.5 ����ˮԡ����37�桫100�档 2.6 ����������5%����+10%������̼+85%����������Ʒ���������� 2.7 ������10×��100×�� 2.8 ������������ϵͳ���������������� 2.9 �����䶳���Ļ���≥12000r/min�� 2.10 С�����Ĺܣ�1.5mL�� 2.11 ����������1μL��1000μL�� 2.12 ��ͷ��������������ƥ�䣩 2.13 PCR�� 2.14 ��¯ 2.15 ��Ӿ�� 2.16 ��Ӿ�����������ϵͳ�����������ǣ� 3 ���������Լ� 3.1 �ʿؾ��꣺�ճ������˾������꣨ATCC 33560�� 3.2 DNA Marker 3.3 ���P����Ƭ�γ��� 3.3.1 ���� �ճ������������� 5’ CAT CTT CCC TAG TCA AGC CT 3’������ 5’ AAG ATA TGG CAC TAG CAA GAC 3’������Ƭ�γ���Ϊ 773bp�� �᳦�����˾������Σ�AGG CAA GGG AGC CTT TAA TC�����Σ�TAT CCC TAT CTA CAA ATT CGCTAT CCC TAT CTA CAA ATT CGC������Ƭ�γ���Ϊ364bp�� 3.4 ���������� 3.5 ������ѡ���ԣ�CCD�������� 3.6 ���ױ���Ѫ��֬������ 3.7 ������ˮ 3.8 10 ×PCR ������Һ�� 3.9 �Ȼ�þ��Һ��25mM�� 3.10 Taq �ۺ�ø��0.5U/μL�� 3.11 dNTPs��2mM�� 3.12 ��֬�� 3.13 50×TAE����Һ����242gTris�57.1mL�����ᣬ100mL0.5M EDTA��pH8.0�����Ӵ�ˮ��1000mL�� 1×TAE����Һ�� ����ʱ��50×TAE����Һ1�ݼ�����ˮ49�ݣ����ȼ��ɡ� 3.14 ��������Һ 3.15 �廯�Ҷ���Һ��10mg/mL������ȡ1g�廯�Ҷ�����100mLˮ�У��ô���������������Сʱֱ����ȫ�ܽ⣬�ܹ���أ�4�棩���档 3.16 ������ 4 �ճ������˾��ͽ᳦�����˾��ķ������������ �ճ������˾��ͽ᳦�����˾��ķ�������������ͼ4�� 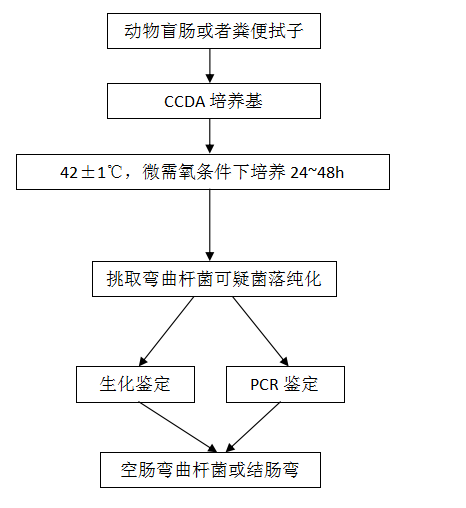 ͼ4 �����˾��ķ���ͼ������� 5 �������� 5.1 �����봿�� 5.1.1 ���� �����ʻ��������������еķ�����ӻ�ä����������CCD��������ͿĨ���þ������������ȴ�Ľ��ֻ���ͿĨ����ֱ���ߡ� 5.1.2 ���� ���������ֺ��ƽ������42��±1������������У�����������������24h��48h�� 5.1.3 ���� �۲�24h������48h��������֬ƽ���ϵľ�����̬����ȡ��ɫ��ʪ���𡢹⻬Բ��Ե����Ŀ��ɵ����䣬��3.2�������������������� 5.2���� 5.2.1�������� �����Ѵ����ľ��䣬��ʹ��������������ϵͳ�������������������������������н���ж�������ͨ��5.1��5.4��������з�������ѧ��PCR�������� 5.2.2 ��������ѧ��PCR������ �ý��ֻ��Ӹ��ױ���Ѫ��֬����������ȡ�����Ĵ�����������ʢ��0.5mL������ˮ��С�����Ĺ��У�12000r/min����2min�������塣�ټ�0.5mL���ˮ���������������ȣ�100���ˮ�����10min��ȡ�����ڱ�ԡ����ȴ5min��12000r/min(4��)����2min��ȡ������ΪPCRģ�塣 5.2.2.1 PCR��Ӧ��ϵ ���ݲ�ͬ����PCR�Լ�����������PCR��Ӧ��ϵ��ͬʱ�������Ժ����Զ��ա� 5.2.2.2 PCR��Ӧ���� ���õ�PCR��Ӧ�������±��� PCR��Ӧ�����
5.2.2.3.1 1.0%��֬����������Ʊ� ��ȡ1.0g��֬�ǣ�����100mL0.5×TBE����Һ����1×TAE����Һ���С������ڻ����5μL��10mg/mL���廯�Ҷ������Ⱥ��������ˮƽ̨���ϵ��������У������5mm���ҡ�������Ʒ��ѡ�����˵����ӡ���������ȴ���̺�γ����ӣ������γɼ����ף��������Ӿ���У���0.5×TBE����Һ����1×TAE����Һ����û���档 5.2.2.3.2 ���� ȡ10µLPCR���������3µL��������Һ���Ⱥ����һ�������ס�ÿ�ε�Ӿ�����Զ��պ����Զ��յ����������1����Ϊ���ա� 5.2.2.3.3 ��Ӿ���� ��ѹ110V����Ӿʱ��40min�� 5.2.2.4 ����ж� ��Ӿ������ȡ����������������Ͷ�����ϴ�����ƹ۲�������������ǽ��г�������� ���ijһ������Ʒ���������������ճ����������Զ��յ�������һ��ֱ���ϣ�������������ľ�����ͬ�������Ʒ���뵽�ľ�����ж�Ϊ�ճ������˾��������᳦���������Զ��յ�������һ��ֱ���ϣ�������������ľ�����ͬ�������Ʒ���뵽�ľ�����ж�Ϊ�᳦�����˾��� ��Ҫʱ������ͨ����������һ��ȷ֤�� �塢 ����Դʺ������ͷ೦����ķ������������ 1 ��Χ �������涨�����ڶ���Դʺ������ͷ೦�������������ķ����� �����������ڸ��ֶ�����ʺ������ͷ೦����ķ���������� 2 �豸�Ͳ��� ������ʵ���ҳ�������������豸�⣬�����豸�Ͳ������¡� 2.1 ���䣺2�桫4���-20�档 2.2 ���������䣺36��±1�档 2.3 ������ƽ������0.1g�� 2.4 ������10×��100×�� 2.5 ���ﰲȫ�� 2.6 ��������������Ʒ�������� 2.7 �����ܻ���Ʒ�����������ӡ� 2.8 ����������1μL��1000μL�� 2.9 ��ͷ������������ƥ�䣩�� 3 ���������Լ� 3.1 ������������ 3.2 �������ɫ�������� 4 ʺ������ͷ೦���������������� ʺ������ͷ೦�����������������ͼ5��  ͼ5 ʺ������ͷ೦���������������� 5 �������� 5.1 ���� ѡ����ֳ�������׳�����������Ӳɼ�������Ż�йֳǻ��Ʒ�����������������У�����ʱ�䲻����48Сʱ�� 5.2 ʺ������ͷ೦����ķ��� 5.2.1 ���ӽ����ڳ������ɫ��֬ƽ�壬36��±1������18��24h�� 5.2.2 ��ȡ��ɫ���Ϻ�ɫ�Ŀ��ɾ��䣬��ɫ��֬�ϴ���һ���� 5.2.3 ��������ɾ������Ӫ����֬ƽ�崿����36��±1������16��18h������һ��ϸ�������� 5.3 ʺ������ͷ೦����ļ��� �����Ѵ����ľ��䣬��ʹ��������������ϵͳ���������������������������ж������ ��Ҫʱ�����ó������Ѫ�����Ѫ���ͼ����� ��������Դκ������������������ 1 ��Χ �������涨������Դκ�������Clostridium perfringens���ķ���������� ����������������Դκ������ķ���������� 2 �豸�Ͳ��� ��Ҫ����Ҫ�豸�Ͳ������£� 2.1 ��Ʒ�������ܻ������ǩ�� 2.2 ��ͨ���䣺2 �桫4���-20�棻 2.3 �����±��䣺-80�棻 2.4 ���������䣺37�棻 2.5 ����ˮԡ����37�桫100�棻 2.6 ���ﰲȫ�� 2.7 ��ƽ������0.1 g�� 2.8 ������10×��100×�� 2.9 ������������ͷ��1μL-1000μL�� 2.10���ֻ�������룻 2.11 ���Ĺܣ�2mL��5mL�� 2.12 �Թܣ�18mm×180mm�� 2.13 ������ֱ��60 mm��ֱ��90 mm�� 2.14 �������ޣ�������������վ������ɷ֣�88%N2��7%H2��5%CO2�� 2.15 �ܷ������ޣ� 2.16�����������������ܷ�ޣ������չ��е�ȫ��O2��ͬʱ����Լ21%��CO2�� 2.17 ��������վ�� 2.18 PCR�ǣ� 2.19 ��¯�� 2.20 ��Ӿ�ǣ� 2.21 ��Ӿ�����������ϵͳ�� 3 ���������Լ� 3.1 ���������� 3.2 Һ�����Ҵ�������������FTG�� 3.3 ����-��������-��˿���ᣨTSC����֬ 3.4 ���Ľ�Һ��BHI����֬ 3.5 ����Ѫ��֬ƽ�� 3.6 P-15B D-��˿���� 3.7 ���Һ��ʯ�� 3.8 ��������ˮ 3.9 ���嶯��-������������ 3.10 �����λ�ԭ�Լ� 3.11 ����-���������� 3.12 ����ţ�������� 3.14 ������ȾɫҺ 3.15 �����λ�ԭ�Լ� �Լ��ף�������������Һ���Լ��ң�α-����������Һ�� 3.16 ��Ʒ��ϸ��DNA��ȡ�Լ��� 3.17 �ʿؾ��꣺�೦��� ATCC29212�����ɫ������� ATCC29213 3.18 DNA Marker��2000bp�� 3.19 Taq DNA �ۺ�ø 3.20 dNTPs 3.21 ��֬�� 3.22 50×TAE����Һ 242g���Ǽ��������飨Tris���57.1mL�����ᣬ100mL 0.5M EDTA(pH8.0)���Ӵ�ˮ��1000mL 3.23 1×TAE����Һ ��ʱ���ǽ�50×TAE����Һ1�ݼ�����ˮ49�ݣ����ȼ��ɡ� 3.24 ����Ⱦ�� 3.25 16S rDNAͨ�����Ԥ�������Ӵ�СΪ1500bp�� ����Ϊ27F��AGAGTTTGATCCTGGCTCA ����Ϊ1492R: GGTTACCTTGTTACGACTT 4 κ������ķ������������ 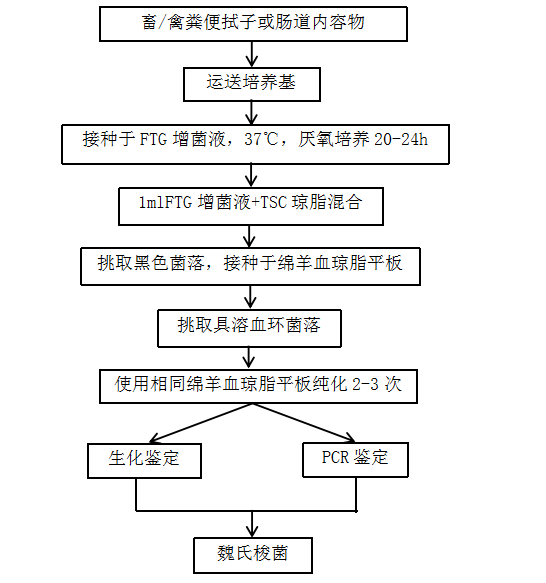 ͼ6 κ������������������ 5 �������� 5.1 ���� 5.1.1 �����ӻ�йֳǻ���ӣ����ò���������ֳ�������׳������������Ľ�����/�ݻ���/�ݸ��壬������ǩ��������Ż�йֳǻ�ɼ���㣬�ɼ��Ľ�����/���뷢����/�ݵ���Ʒ����Ϊ1:1������������������ 5.1.2 �����Ʒ�����ò���������ֳ�������׳������������Ľ�����/�ݻ���/�ݣ�������ǩպȡ����й�����ʷ�㣨��������Ӱǿ�����Ƥ��պȡ�ڲ���㣩������������������ 5.1.3 ������������ò���������ֳ�������׳������������������ʼ���/�ݣ�����ȡ������/�쳣���Σ�ä����᳦�Σ����������������Է���� 5.1.4 �������ɼ�����Ʒ�����ñ�ע���������ڴ��б����ı����豸�У�ת���������ң�ת��ʱ�䲻����48h���� 5.2 �����ͷ��봿�� 5.2.1 �������� ��1�������Ӻͷ����Ʒ����ʢ����Ʒ����������������ȡҺ��200μL�����뺬2mL FTG��5mL���Ĺ��У��������Һ��ʯ����סҺ�棬������������վ���ܷ��������У�37 ����������20-24 h���������� ��2��������������������Σ��ý��ֻ���ȡ����� ���뺬2mL FTG��5mL���Ĺ��л��ȣ���ʯ����סҺ�棬������������վ���ܷ��������У�37 ����������20-24 h���������� 5.2.2���봿�� ��ȡ����Һ1mL����90mm��ƽ���ڣ�ÿ��ƽ����ע��ȴ��50 ���TSC 15 mL�����ȡ���֬���̺��ټ�10 mL ��ȴ��50 ���TSC���ȸ����ڱ��㡣����֬�ٴ����̺�����������վ���ܷ��������У�37 ����������20-24 h����ȡ��ɫ�������ɫ��Ȧ�ĵ��������������Ѫ��֬ƽ���ϣ�������������վ���ܷ��������У�37 ����������20-24 h����ȡ����Ѫ���ľ��䡣����ͬ����Ѫ��֬ƽ�崿��2-3�Ρ� 5.3 κ��������� 5.3.1 �������� ������Ѫ��֬ƽ������ѡ5 ����С��5 ��ȫѡ������Ѫ���ľ��䣬�ֱ���ֵ�FTG ��������������������վ���ܷ��������У�37 ����������20-24 h�� 5.3.2 ��̬�۲� ��ȡ������и�����Ⱦɫ������۲�ϸ����̬��κ�����Ϊ���������Դ̸ֶ˾�������ɫ����ʱ�ɼ�ѿ���塣�����̬��������������Һ������Ӧ���߽�������Ѫ��֬ƽ�壬������������վ���ܷ��������У�37 ����������20-24 h����ȡ������������Ѫ���ľ�����ֵ�FTG ��������������������վ���ܷ��������У�37 ����������20-24 h������һ���������Ѵ����ľ�������ں���������������PCR�������顣 5.3.3 ţ����ӿ�������� ȡ������ʢ��FTG ����Һ1 mL �����ں���ţ������������46 ��±0.5 ��ˮԡ������2 h ��ÿСʱ�۲�һ������“���ҷ���”����������ص��������������������γɺ��������ʣ�ͨ�������������������档5 h �ڲ�������Ϊ���ԡ�κ������������ǣ������ҵ��ײ�������������“���ҷ���”��������������ڡ� 5.3.4 �������� ��1�������λ�ԭ—�������� �ý��ֻ����룩ȡFTG ����Һ���̽��ֻ��嶯��-��������������������������վ���ܷ��������У�37 ����������20-24 h��������¼��ϸ���ش����ߵ�����������ж����������ж����ľ����ش����߳���ɢ�����������ľ���ֻ�ش�����������Ȼ��μ�0.5 mL �Լ���0.2 mL �Լ����Լ���������εĴ��ڡ�15 min �ڳ��ֺ�ɫ�ߣ����������α���ԭΪ�������Σ������������ɫ�仯���������п�ۣ�����10 min�����ֺ�ɫ�ߣ������þ��겻�ܻ�ԭ�����Ρ�κ������������ܽ������λ�ԭΪ�������Ρ� ��2�����Ƿ���-����Һ������ �ý��ֻ����룩ȡFTG ����Һ���̽�������-������������������������վ���ܷ��������У�37 ����������20-24 h���۲������緢�ֲ������������ɺ��ƣ��������DZ����Ͳ����ᡣ���Թ���5 �����ҷ���1 h���������Һ�����������������ǹ�̬���ٷ�����������վ���ܷ��������У�37 ����������20-24 h���ظ���������Ƿ�Һ����κ������ܷ������ǣ�ʹ����Һ���� 5.3.5 ��������ѧ��PCR������ ��1��PCRģ���Ʊ� ��FTG��������ȡ0.5-1mL��������������1.5mL���Ĺ��У���ϸ��DNA��ȡ�Լ��в���ָ����ȡ���������DNA����ΪPCRģ�塣 ��2��PCR��Ӧ��ϵ���� �����Ϊ50μL������PCR Taq DNA�ۺ�ø25μL��16S rDNAͨ�������ϡ����θ�1μL��ģ��1μL��dd H2O 22μL���������������Զ��ա� ��3��PCR��Ӧ���� 94��Ԥ���� 5min��94�� 30s��50�� 30s��72�� 1min30s����30��ѭ����72�� 7min���������ﳤ��ԼΪ1500bp�� ��4����Ӿ ��Ӧ������PCR������1.0%��֬��������Ӿ��⣬��Ӿ����Ϊ����ѹ120V����Ӿʱ��25min����Ӿ�����������������ǽ��г�������� ��5������ж� ����Ӿ����ʾ������PCR������ȥ����˾����16S rRNA�������صIJ�������NCBI�ϵ�Blast���бȶԷ����� 5.4 ���ֱ��� ��������ϲ�ȷ����κ������ľ������������Ѫ��֬ƽ���ϣ�������������վ���ܷ��������У�37 ����������20-24 h���������ϵľ���ȫ�����£����ں���500μL FTG��1.5mL���Ĺܣ���500μL���ͣ�60%����ֻ��ȣ�����-80�泬���±��䱣�档 �ߡ�������Ѫ�˾��ķ������������ 1 ��Χ �������涨�˶���Դ������Ѫ�˾��ķ�������������� �����������ڸ�����Ѫ�˾��ķ���������� 2 �豸�Ͳ��� ������ʵ���ҳ�������������豸�⣬�����豸�Ͳ������¡� 2.1 ���䣺2-4���-20�档 2.2 ���������䣺37±1�档 2.3 ������ƽ������0.1g�� 2.4 ������ƽ������0.1mg 2.5 ����ˮԡ����37�桫100�� 2.6 ���ﰲȫ�� 2.7 ������10×��100× 2.8 PCR�� 2.9 ��Ӿ�� 2.10 ��Ӿ�����������ϵͳ�����������ǣ� 2.11 ����������1μL��1000μL 2.12 ��ͷ������������ƥ�䣩 2.13 ϸ����λ������� 2.14 96�װ� 3 ���������Լ� �����꣺������Ѫ�˾�SH0165 �ʿؾ��꣺��Ĥ�����߸˾�ATCC 27090 3.1 ��֧ԭ��̥ţѪ�塣 3.2 �ȵ����˴���֬��TSA�� 3.3 �ȵ����˴�������TSB�� 3.4 Amies���������� 3.5 ��øNAD 3.6 DNA Maker 2000 3.7 Taqmix DNA �ۺ�ø 3.8 ��֬�� 3.9 50×TAE buffer ���Ǽ��������飨Tris�� 242g NA2EDTA.2H2O 37.2g ���� 57.1ml �Ӵ���ˮ�� 1000mL 3.10 16sRNA���� �������� 5’-GGCTTCGTCACCCTCTGT-3’ �������� 5’-GTGATGAGGAAGGGTGGTGT-3’ 4 ������Ѫ�˾�������������� 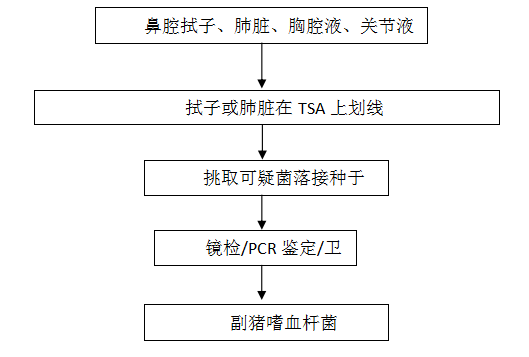 ͼ7 ������Ѫ�˾������������ 5 �������� 5.1 ���� ѡ����ֳ�������׳�����������Ӳɼ������ǻ���ӣ������������������ࡢ�İ�Һ����ǻ��Һ���ؽ�Һ���Լ�Һ����������У�����ʱ�䲻����48Сʱ����ǻ�������ڼ���1%NAD��Amies�����������С� 5.2 ������Ѫ�˾��ķ��� 5.2.1 ���ࣺ�þƾ��ƻ���Է����������������������ļ��������Ӽ�ȡһС�鲡����������ڼ���5%̥ţѪ���10μg/mL NAD��TASƽ���Ե1/4Ϳ�壬�������Ľ��ֻ���ȡ����ʽ��������ϸ�����л��߷���������37������36-48h��ȡ��ǻ�����ڼ���5%̥ţѪ���10μg/mL NAD��TASƽ�������λ��ߣ�37������36-48h�� 5.2.2 ��ȡ��������Ե�⻬�Ŀ��ɾ�����2.5mL����5%̥ţѪ���10μg/mL NAD����TSB������37������18-24h�� 5.2.3 ��������ɾ������Ӫ����֬ƽ�崿����37������36h������һ��ϸ�������� 5.3 ������Ѫ�˾��ļ��� 5.3.1 ���� ��ȡ��������Բ�Ρ��⻬����ɫ�����ɾ���ͿƬ������Ⱦɫ�������¹۲�ϸ����̬��������Ѫ�˾�Ϊ���������Զ̸˾��������С��һ�� 5.3.2 ����ʵ�� �ý��ֻ��ֱ���ȡ�������ɾ��ĵ����䣬ˮƽ������������Ѫ��֬ƽ���ϣ� ����ȡ���ɫ���������ֱ��ˮƽ���ߣ������� ���� ���� �衫���� �裬�۲��Ƿ���“��������”���� 5.3.3 ������Ѫ�˾���PCR���� �ڴ����������TSA ����������ȡ�����䣬�������1% NAD ��5%̥ţѪ����ȵ����˴�����(TSB)�������У�37�棬220 r/min ҡ��������18h���ҡ�ȡ������ľ�Һ1μL��PCR���������Զ���Ϊ������Ѫ�˾��ο���SH0165�����Զ��ղ���ģ�塣���ݸ�����Ѫ�˾�16S rRNA(M75065)�����������ɽ�˹�����\������˾�ϳɣ�����5-1����ȡ20 μL��Ӧ��ϵ����ɳɷּ���5-2����Ӧ����Ϊ��94��Ԥ����5 min��94�����10 s��59���˻�10 s��72������1 min��30 ��ѭ�������72������10 min�� ��1 ������Ѫ�˾�PCR������������
��2 PCR��ϵ�����һ����
��ȡ1g��֬�ǣ�����100mL 1×TAE ����Һ�У��������Ⱦ�ϣ�������Ʒ��ѡ�����˵����ӣ���֬���ܻ�����ȵ�����ˮƽ̨���ϵ��������У������5mm���ҡ���������ȴ���̺�γ����ӣ�ȡ����������Ӿ���У���1×TAE����Һ��û���档 ȡ10µLPCR���������3µL��������Һ���Ⱥ��������ף�ÿ�ε�Ӿʱ������һ�����Զ��պ����Զ��ա���Ӿ��������ѹ110V����Ӿʱ��30min�� ����ж�����Ӿ������ȡ��������������Ͷ�����ϴ�����ƹ۲�������������ǽ��г�����������ijһ������Ʒ��������������븱����Ѫ�˾����Զ��յ�������һ��ֱ���ϣ�������������ľ�����ͬ�������Զ����������������Ʒ���뵽�ľ���ɳ����ж�Ϊ������Ѫ�˾��� 5.4 ������Ѫ�˾��ı��� �ڴ������ƽ������ȡ��������8mL�����У�����37��ҡ��������18~24h������Һ�����������ڣ���9000r/min������3���ӣ���ȥ����Һ������4mL�������֬ţ�̣��������ٷ�װֵ����Ķ��ɹܣ�ÿ��1mL���ٽ���װ�ľ��������䶳���Ⱥ�����4�棬-20�棬-80������4h���ϡ����Һ���ڶ��ɻ�����1~2�죬���ɺ�����-80����䳤�ڱ��档 �ˡ�����Դα��˰�״�˾��ķ������������ 1 ��Χ �����涨�˶���Դα��˰�״�˾��ķ������������ ����������ŧ֭��α��˰�״�˾��ķ������ 2 �豸�Ͳ��� ������ʵ���ҳ�������������豸�⣬�����豸�Ͳ������£� 2.1 ���ﰲȫ�� 2.2 ���䣺0 �� ~ 4 �� �� -20 �� 2.3 ���������䣺36 �� ± 1 �� 2.4 ������10 ×~ 100 × 2.5 EP��:1.5 ml 2.6 ������ 2.7 ���������� 2.9 �������� 2.10 ��ͷ ��������������ƥ�䣩 2.11 PCR�� 2.12 ��¯ 2.13 ��Ӿ�� 2.14 ��Ӿ�����������ϵͳ�����������ǣ� 3 ���������Լ� 3.1 DNA Marker 3.2 ���P����Ƭ�γ��� PLD������� ���Σ�CTCAAGGCGTGGATGA ���Σ�GGTAGCCAGATGGTGAGTAG 3.3 ���������� 3.4 10 ������������Ѫƽ�� 3.5 2×Taq PCR MasterMix ����Ⱦ�ϣ� 3.6 ��֬�� 3.7 50×TAE����Һ����242 g Tris �57.1 ml �����ᣬ100 ml 0.5M EDTA��pH 8.0�����Ӵ�ˮ��1000 ml�� 1×TAE����Һ������ʱ��50×TAE����Һ1�ݼ�����ˮ49�ݣ����ȼ��ɡ� 3.8 �廯�Ҷ���Һ��10�J/ml������ȡ1 g�廯�Ҷ�����100 mlˮ�У��ô���������������Сʱ����ȫ�ܽ⣬�ܹ���أ�4 �棩���档 4 α��˰�״�˾��������������  ͼ8 α��˰�״�˾������������ 5 �������� 5.1 ���� ����ȡŧ֭��Ʒ���������������У�0 ��—4 �汣�档 5.2�����봿�� 5.2.1 ���� �����ʵĻ������������е�ŧ֭������10����������Ѫ��֬ƽ����ͿĨ���þ������������ȴ�Ľ��ֻ����ߡ� 5.2.2 ���� ���������ֺ��ƽ������37 �� ����������������24h~48h�� 5.2.3 ���� �۲�24h��48h��Ѫ��֬ƽ���ϵľ�����̬����ȡԲ�Ρ�����������ɴࡢ�ɰ�ɫ��ɫ������Ѫ�������խα��Ѫ��С���䰴5.2.2��������������������������Ⱦɫ������С��˾��� 5.3���� 5.3.1 �������� �����Ѵ����ľ��䣬��ʹ��ϸ����������Ӧ�ܽ������������������ա�������ϸ�������ֲᡷ���н���ж��� 5.3.2 PCR���� 5.3.2.1 PCRģ����Ʊ� �ý��ֻ���Ѫƽ������ȡ�����Ĵ�����������ʢ��0.5 ml������ˮ��С�����Ĺ��У�12000r/min���������ӣ������塣�ټ�0.2ml���ˮ�������ȣ�100��ˮԡ10min��12000r/min���������ӣ�ȡ������ΪPCRģ�塣 5.3.2.2 PCR��Ӧ��ϵ ���ݲ�ͬ����PCR�Լ�����������PCR��Ӧ��ϵ������Ŀ��Ƭ�γ���Լ758 bp. 5.3.2.3 PCR��Ӧ���� 94 ��Ԥ����2min��94 �����30s��54���˻�30s��72������50s��30��ѭ�������72��������10min��ͬʱ�������Ժ����Զ��ա� 5.3.2.4 ��Ӿ ��ȡ1.0g��֬�ǣ�����100ml 1×TAE����Һ�������ۻ�����ˮƽ̨����������У������Լ5 mm��������Ʒ��ѡ�����˵����ӡ��������̺����Ӿ�ۣ��ڼ������м������� DL2000Ϊ���գ�120v��30min �����廯�Ҷ���Һ�н���20min��֮����������������ϵͳ������Ͷ�����й۲����� 5.3.2.5 ����ж� ���ijһ������Ʒ���������������α��˰�״�˾����Զ��յ�������һ��ֱ���ϣ�������������ľ�����ͬ�������Ʒ���ж�Ϊα��˰�״�˾�����Ҫʱ��ͨ��16S rRNA������н�һ����֤�� ����3—6 ҩ���������Լ���ʹ�ã�MIC�ⶨ���������� 1 ��Χ �������涨�˶���Դϸ�����˾���ɳ���Ͼ�������������ɫ���������������Ѫ�˾���κ�������α��˰�״�˾���ҩ������Լ��еIJ��������� 2 ���� ������ʵ���ҳ�������豸�⣬�����豸�Ͳ������£� 2.1 ����������35±2�� 2.2 ���ﰲȫ�� 2.3 �Ƕȼƻ��߱����ǹ� 2.3 ��������1uL~1000uL 2.4 ��ͷ������������ƥ�䣩 3 �������� ȡ���Լ��У���װ���á� ��Һ�Ʊ� ������ǩ��������ˮ��ʪ��ֱ��ȡ��ҹ���������������ʾ��䣬��������������ˮ���ȡ�Ȼ���ñ����ǹܻ����Ƕȼ�У����ҺŨ����0.5���ϵ�λ��1~2×108CFU/mL����������Լ����е���������ʹ��˵����Ҫ��ı���ϡ�ͣ����ȱ��á� ��Һ���� ���հ����⣬�����95�����Ʊ��ã���ǰҪ���ȣ��ľ�Һ100µL �հ��տ��м���100µL���������Ǻð�Dz���¼���š� ���� ����������35��±2������������з���16~18Сʱ�� �۲��� �ڳ��кڵװ�Ĺ����£������۹۲졣 �ȹ۲����Զ��տ����Զ��տף����Զ��տ�Ӧ��ϸ������������Һ��δ�����ǣ����Զ��տ���Ӧ��ϸ���������γɵ�Բ�λ�����״������ ������Ժ����Զ��ս�������������۲��������ϸ���������������ϸ�������Ŀ���������Ϳ���ҩ��Ũ�ȼ�Ϊ����־�Ũ�ȣ�MIC���� 4 �����¼ ��MIC�����¼�������Լ����ͳ�Ʊ��С�
�����Լ����ͳ�Ʊ�
��1��G-�����˾���ɳ���Ͼ�������Ѫ�˾���MIC
��ֳ���� ���Ա�� �� �� ��
��2��G+��������������ɫ���������α��˰�״�˾���MIC
��ֳ���� ���Ա�� �� �� ��
��3�������˾�MIC
��ֳ���� ���Ա�� �� �� ��
��4���������κ�����MIC������������ҩ���⣩
��ֳ���� ���Ա�� �� �� ��
����4
2020��������������ȫ���ƻ�
���ݡ���Ʒ������ȫ�ල�����������涨����֯��չ2020��������������ȫ���ƻ����й�����Ҫ�����¡�һ����ʵ����������������ȫ����������� ����������ҽ����ҵ�����ܲ���Ҫ�ϸ��ա�ʳƷ��ȫ��������Ʒ������ȫ�ල�������������ط������ɲ�ʳƷ��ȫ�����ƹ涨���ȷ��ɷ���淶���ļ��Ĺ涨�������ؼ����ϵط����������Ա�����������������������ȫ�����𣬸���������ҽ����ҵ�����ܲ��Ÿ�������Σ�������ֳ�ߡ��������չ�վ�����ߺ����䳵��Ӫ�߸���һ���ε�Ҫ��������ʵ�������Ρ���ʡ�������У�������ҽ����ҵ�����ܲ���Ҫ��������ƶ���ʵ��ʡ�������У���������ƻ���ʵ���չ�վ�����䳵��ȼ��ȫ���ǣ�������ܿհס� ������ǿ�������չ����价�ڼ�� ����Ҫ��ǿ���������չ�վ�����䳵�ļ�ܣ�ȷ��Ͻ���ڰ䷢֤�գ��������ɣ����������չ�վ�����䳵�߱������������������ڲ������������չ�վ�����䳵�������ȡ�ޣ����������Ϣ�����������֤�չ�������Ϊ����ʡӪ�����䳵�����ܷ�֤���������ؼ�ܣ�Ҳ��Ӫ�˵��������ؼ�ܡ��Ϸ����ϸ��������г����Բ��ϸ���Ʒ��������е��������λҪ�ڼ�������鴦����3���������ڱ����й�ʡ��������ҽ����ҵ�����ܲ��š������������Υ��Υ��������Ϊ������һ�𣬲鴦һ���������·���ģ���ʱ���������ţ������ٲ鴦�����ʱ�����Ҳ�������ҽ����ҵ���� �����ƽ���Ϣ�����������������������ȫ�����Ч�� ����Ҫȫ������“ȫ���������չ�վ���䳵�ල����ϵͳ”�� ����ר�˸���Ͻ�����������չ�վ�����䳵��Ϣ�˲��ϱ���������ʱ���������Ϣ��ȷ����Ͻ������վ�����䳵��Ӥ���䷽�����Դ���ر仯�������ǿ��ܼ�����Ӳ���������裬ȫ���ƽ����������չ�����֤������������֤�������߳�֤����߹����淶��ˮƽ����չ“�������ƶ������ն�”��“�������չ�վ���䳵�ֳ�����ƶ��ն�”Ӧ���Ե㣬���ܼ�����Ϣ��������ˮƽ���ӿ�������������ȫ�����ݿ⽨�裬�ƽ���Ϣ��Դ�����빲����Ϊ��ܹ����ṩ����֧�š� �ġ���ǿ��֯Э�������ϼ�ܼ�������չ ��֪ͨ�´�����������������辭�����Ҳ�2020��������������ȫ��ܲ���ר��Ѱ��š��Ҳ�ί��ũҵũ�岿�̼�����Ʒ�����ල����������ģ��������е��������λ�ļ��������֤�ȶԿ��ˡ�������е���λҪ���ݼ�����Ҫ���μӼ�⼼����ѵ�����������豸���ã��������Ŀ�ѧ�Ժ�ȷ�ԡ���ʡ�������У�������ҽ����ҵ���������ܲ���Ҫ�߶�����������������ȫ��������ʵ��ǿ��֯�쵼��Э�������ø������ϵ�����ʱ�����ɼ����������2020��4��25��ǰ����ʡ2020��������������ȫ���ƻ����Ҳ�������ҽ����ҵ�������� ��ϵ��ʽ ũҵũ�岿������ҽ����ҵ�� �绰��010-59191536/46 ���棺010-59191533 �����ʼ���nzzd@agri.gov.cn �йء�������������ȫ���ϵͳ�����������չ�վ���䳵�ල����ϵͳ����“�������ƶ������ն�”��ʹ����ϵ�й�ũҵ��ѧԺ����������ҽ�о��� �绰��010-62160212 ���棺010-62160213 �����ʼ���67513193 @qq.com ������4—1. 2020��������������ȫ���ƻ���¼ 4—2. 2020��������������ȫ�ල���ƻ���¼ 4—3. ũҵũ�岿������������ȫ�����淶 ����4—1
2020��ȫ�����������м��ƻ������
����4—2
2020��Ӥ���䷽�����Դ������ȫ���ƻ������
����4—3
2020��������������ȫ���г��ƻ������
(���α༭��admin) |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
ũҵũ�岿����ӡ��2020��������ҩ������������ȫ���ƻ���֪ͨ
ʱ��:2020-05-15 15:18��Դ:ũҵũ�岿��վ ����:admin ���:
��
------�ָ���----------------------------
- �Ƽ�����
-
- ��������2015�桶�й���ҩ�䡪��ҩ��Ʒ˵...
���йص�λ�� 2015�桶�й���ҩ����ҩ��Ʒ˵���鷶���������¼�Ʒ���������ҩ��Ʒ��...
- ��ҩ�����2018������Ʒѧ����̳֪ͨ
�й�����ѧ����ҽ����ѧרҵίԱ�� ���й�������ҽѧ��������Ʒѧ 2018��ѧ����̳...
- ��������2015�桶�й���ҩ�䡪��ҩ��Ʒ˵...
- �ȵ�����
-
- �й���ҽҩƷ��������ھٰ������й���...
- ��������2015�桶�л�������ҩ�䡷...
- ũҵ���칫��������ҩ��Ʒ�����й������...
- ���ھٰ��һ�ڡ��й���ҩ�䣨2015�棩��...
- ũҵ���칫��������ҩ��Ʒ���ĺź˷���...
- ���ھٰ�ڰ˽��й���ҩչ�����֪ͨ
- �л�����ũҵ������ ��2223��
- �����ٿ���ҽ����ѧרҵίԱ���������...
- ��������2015�桶�й���ҩ�䡪��ҩ��Ʒ˵...
- ���ڽ�����ҩע��Ǽ���������֤�շѽɿ�...





